【講演会演者】重症喘息治療における意思決定支援

2026.3.7に東京(京橋)で行われました重症喘息に関する講演会に演者として参加致しました。
以下、聴講録となります。ご興味がある方はご覧ください。
近年、重症喘息治療は大きく変化している。その中心にあるのが生物学的製剤(biologics)の登場である。従来、重症喘息の治療は高用量ICS/LABA、LAMA、LTRA、テオフィリン、経口ステロイド(OCS)などを組み合わせながら行われてきた。しかし、これらの治療を最大限に行ってもなお症状コントロールが不十分で、増悪を繰り返し、しばしば全身ステロイド投与を要する患者が一定数存在する。このような患者群が重症喘息(severe asthma)と定義される【1】。生物学的製剤の登場により、これまでOCSに依存せざるを得なかった患者に対して、増悪抑制や症状改善、QOL改善、さらにはOCS sparingを目指す新たな治療戦略が可能となった。一方で、生物学的製剤は高価であり、適応判断も複雑で、患者ごとにフェノタイプや併存症、社会経済的背景を踏まえた個別化医療が求められる。したがって、重症喘息治療においては、単に“良い薬を勧める”のではなく、患者が自身の病状と治療選択肢を理解し、納得して治療を選ぶための意思決定支援が極めて重要となる。
当院における重症喘息診療
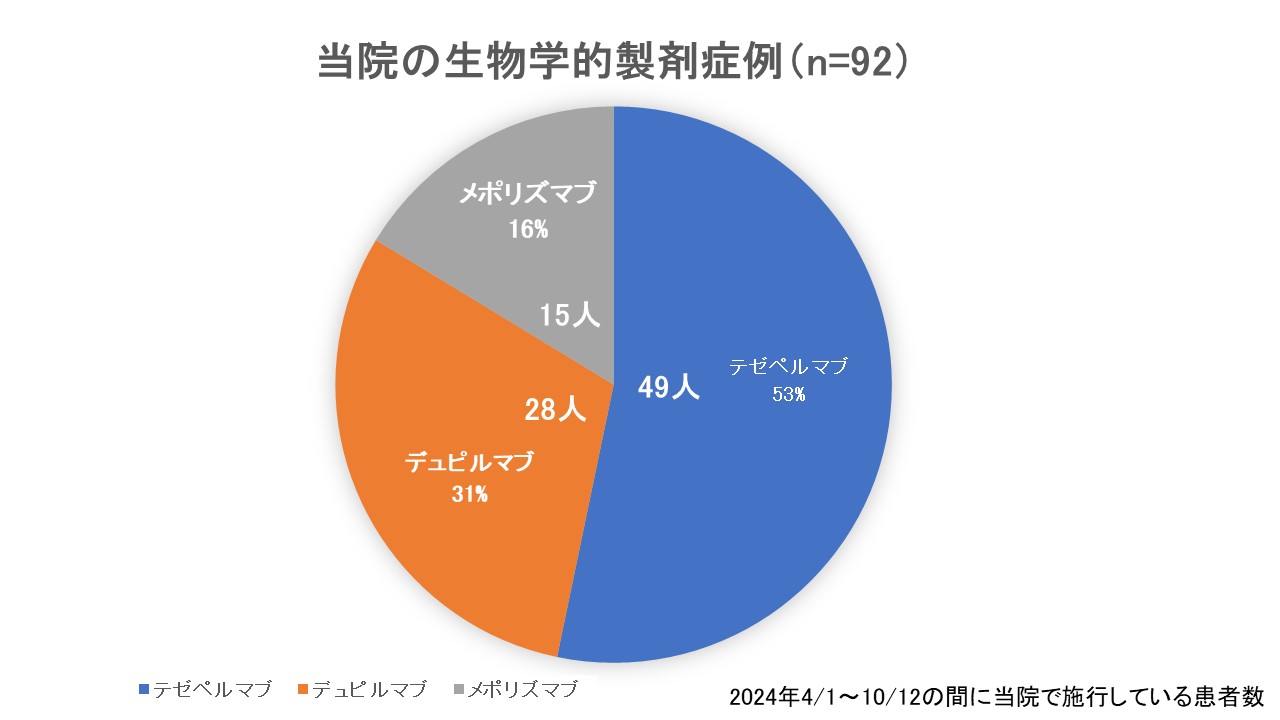
当院は東京都江戸川区葛西駅前に位置する呼吸器内科クリニックであり、外来診療を中心に喘息診療を積極的に行っている。診察室13室を有し、医師、看護師、医療事務、医師事務作業補助者を含む多職種体制で診療にあたっている。重症喘息に対する生物学的製剤治療にも力を入れており、2025年2月時点で約100名の患者に導入している。実臨床では、テゼペルマブ、デュピルマブ、メポリズマブを中心に使用しており、患者背景やフェノタイプ、併存する副鼻腔疾患の有無、費用面などを考慮して薬剤選択を行っている。たとえば、ECRSを伴う症例ではデュピルマブが有力な選択肢となり、好酸球優位で増悪反復が中心の患者ではIL-5阻害薬が候補となる。一方、好酸球数にかかわらず幅広く適応を考えたい症例ではテゼペルマブが選択肢に入る。こうした薬剤選択は、単純な数値だけではなく、患者の生活背景や治療受容性も含めて総合的に判断する必要がある。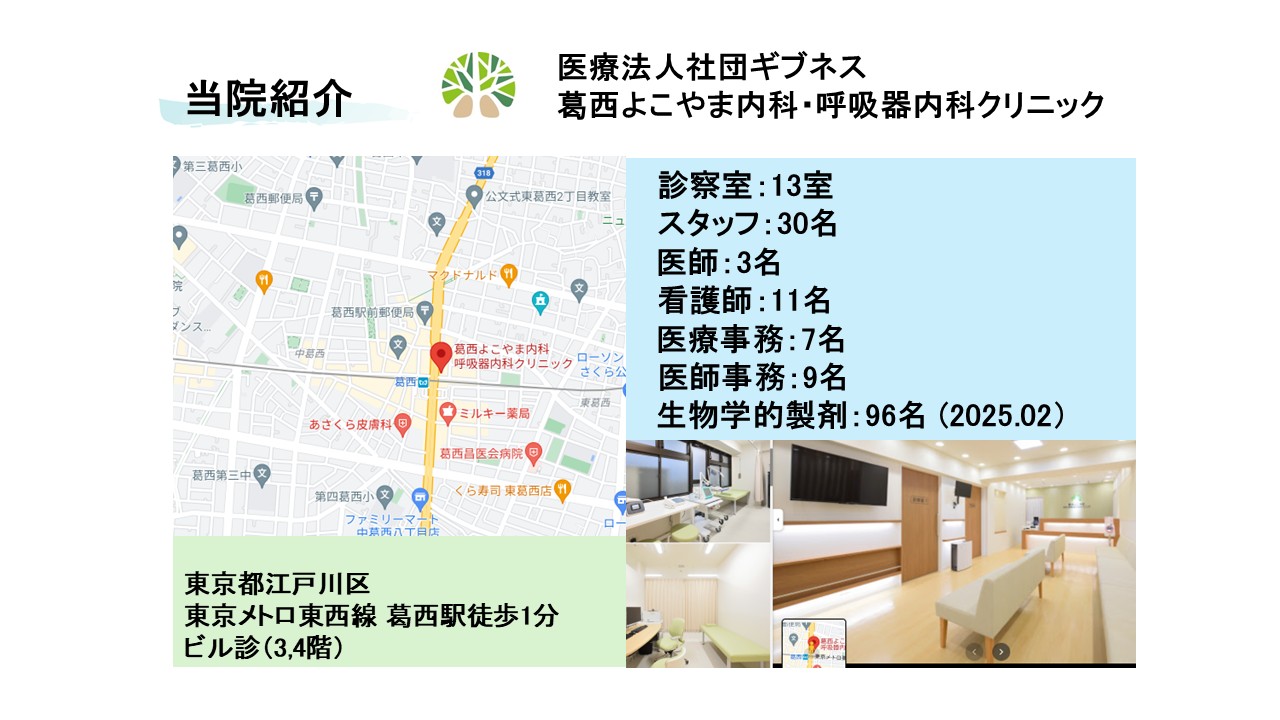
重症喘息の疫学
喘息は世界的に極めて頻度の高い慢性呼吸器疾患であり、世界では約3億人が罹患していると推定されている【2】。日本でも有病率はおおむね8%前後とされ、推定患者数は約1000万人規模に及ぶ。一方で、そのすべてが重症ではなく、多くの患者は標準治療によって良好なコントロールが得られる。重症喘息は喘息患者全体の約5〜10%とされるが、この一群が医療資源消費、QOL低下、増悪、入院、OCS曝露の多くを占めることが知られている【1】。外来診療の感覚としても、一般喘息患者100人のうち5〜10人前後が重症喘息に該当するイメージであり、決して稀ではない。しかも、重症喘息患者は単に“症状が強い患者”ではなく、繰り返す増悪や併存症、治療アドヒアランスの問題、吸入手技、社会的背景、心理的要因などが複雑に絡み合うことが多い。そのため、重症喘息診療はガイドラインに従った単純な治療強化だけでは不十分で、総合的・多面的な評価が不可欠である。
重症喘息の臨床的問題
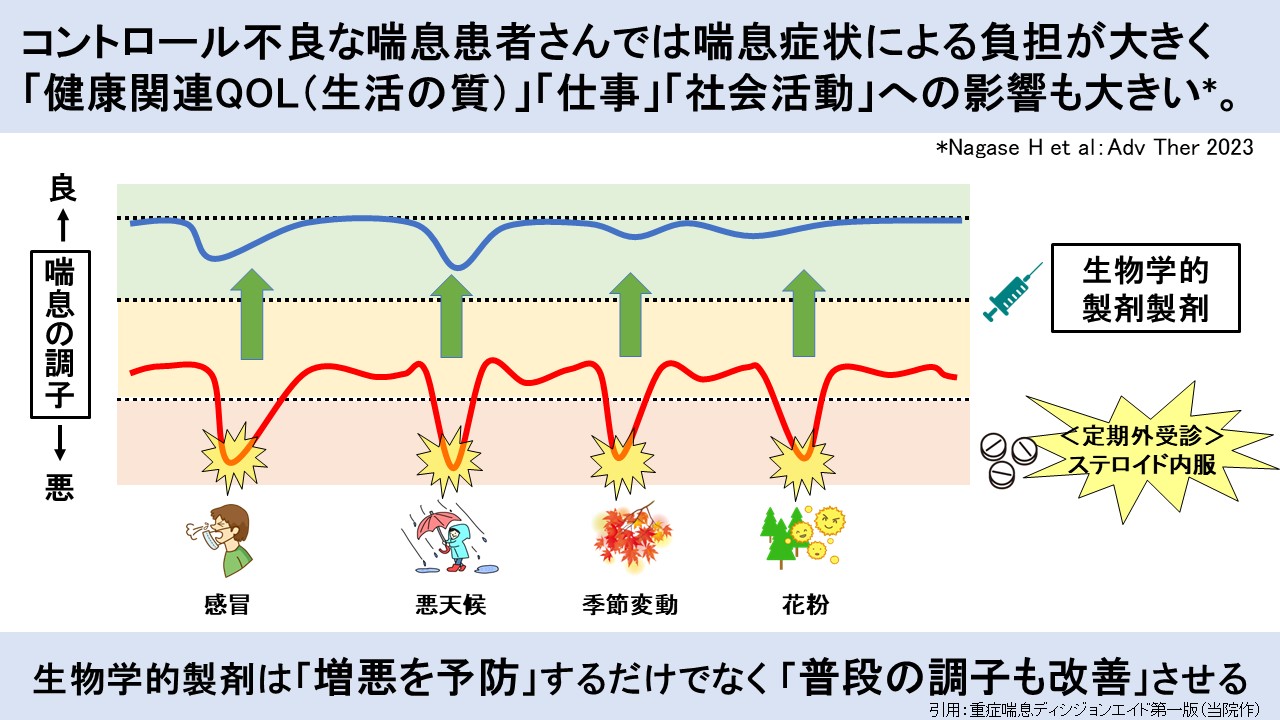
重症喘息患者では、咳嗽、喘鳴、呼吸困難、胸部圧迫感、夜間覚醒といった症状が持続し、日常生活に大きな支障をきたす。階段昇降や通勤、家事、育児、運動といったありふれた活動が制限されるだけでなく、夜間症状による睡眠障害、翌日の倦怠感、集中力低下、労働生産性低下など、生活のあらゆる側面に影響が及ぶ。さらに、感冒、花粉、天候変化、気温差、黄砂、PM2.5などを契機に増悪し、救急受診や時間外受診を要することも少なくない。こうした患者の中には、普段から症状を抱えながらも「悪くなったらOCSを飲めばなんとかなる」と認識している方が少なくない。しかし、これは結果として増悪の反復とOCS依存を強化し、長期的には肺機能低下や副作用蓄積につながる可能性がある。したがって、重症喘息の問題は“今つらい”ことだけではなく、“このままでは将来さらに悪くなる”ことにある。この時間軸の違いを患者と共有することが、意思決定支援の出発点となる。
喘息増悪と肺機能低下
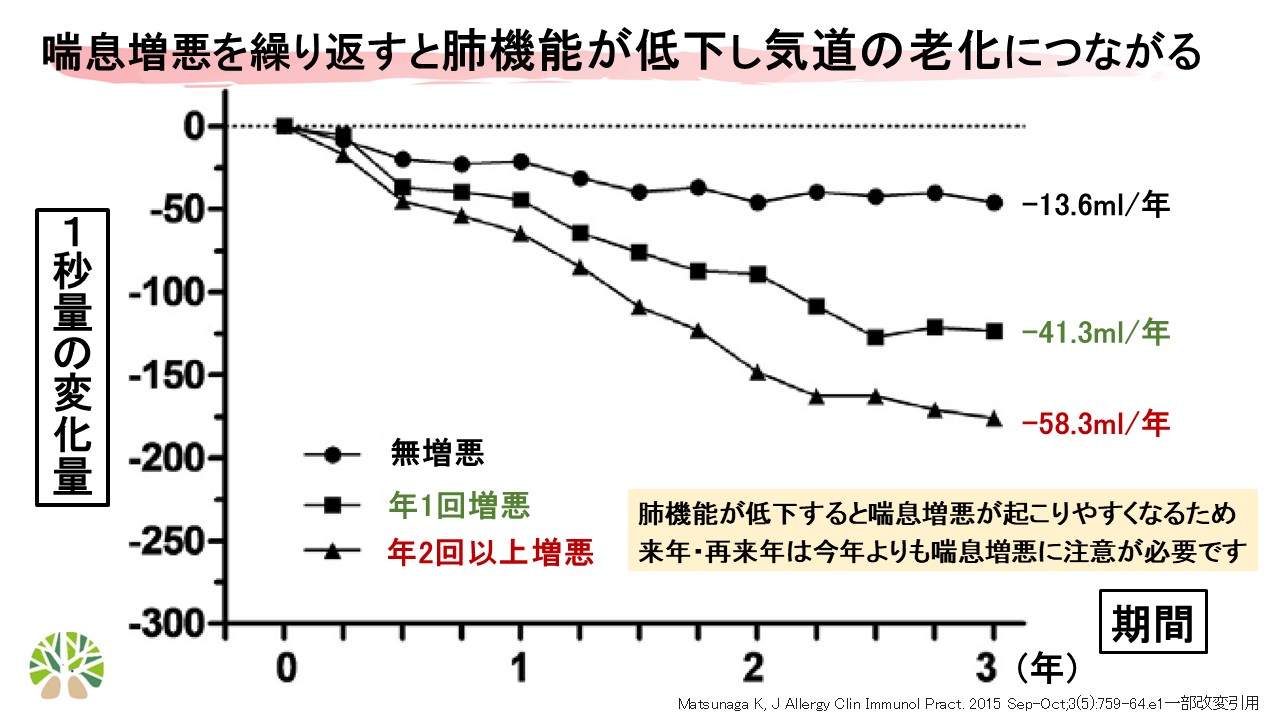
喘息増悪は一過性イベントとして捉えられがちであるが、長期予後の観点からは極めて重要である。増悪を繰り返す患者では肺機能低下が加速することが報告されており、Matsunagaらは増悪頻度と1秒量(FEV1)低下速度の関連を示している【3】。増悪のない患者に比べ、年1回増悪する患者、年2回以上増悪する患者では、年間のFEV1低下がより大きくなり、将来的な呼吸機能障害の進行が懸念される。このことは、増悪を単なる“その場しのぎで治すイベント”ではなく、“気道の老化を進める重要な転換点”として捉える必要があることを意味する。増悪後に症状が改善したとしても、それで元通りというわけではない。むしろ増悪のたびに気道リモデリングが進み、翌年・再来年のコントロールがさらに難しくなる可能性がある。したがって、重症喘息治療では「普段の症状を軽くする」ことに加え、「増悪を予防する」ことが極めて重要となる。
OCS依存の問題
重症喘息患者では、増悪時に経口ステロイド(OCS)がしばしば使用される。OCSは短期間で強力な抗炎症作用を発揮し、多くの患者で症状改善をもたらすため、医療者側にとっても患者側にとっても“効く薬”として認識されやすい。しかし、その即効性ゆえに、長期的な副作用リスクが軽視されやすいという問題がある。Dalalらは、OCS使用と複数の有害事象リスク増加の関連を報告しており、骨粗鬆症、糖尿病、心筋梗塞、脳卒中、感染症、白内障、緑内障、うつ病など多彩な合併症が問題となる【4】。しかも、これらの有害事象は高用量・長期投与だけでなく、中等量あるいは比較的少量の反復投与でもリスクが上昇することが示されている。重症喘息患者において、OCSは“必要な時に使う薬”ではあるが、“繰り返し使ってよい薬”では決してない。実際、患者はOCSを飲むと楽になる経験を何度も重ねるため、「今までこれで良くなってきたから今回も同じでよい」と考えやすい。しかし、症状緩和と長期安全性は別問題である。重症喘息診療では、OCSの有効性を認めつつ、その代償として生じる長期リスクを適切に説明し、可能な限りOCS曝露を減らす方向に治療を組み立てる必要がある。
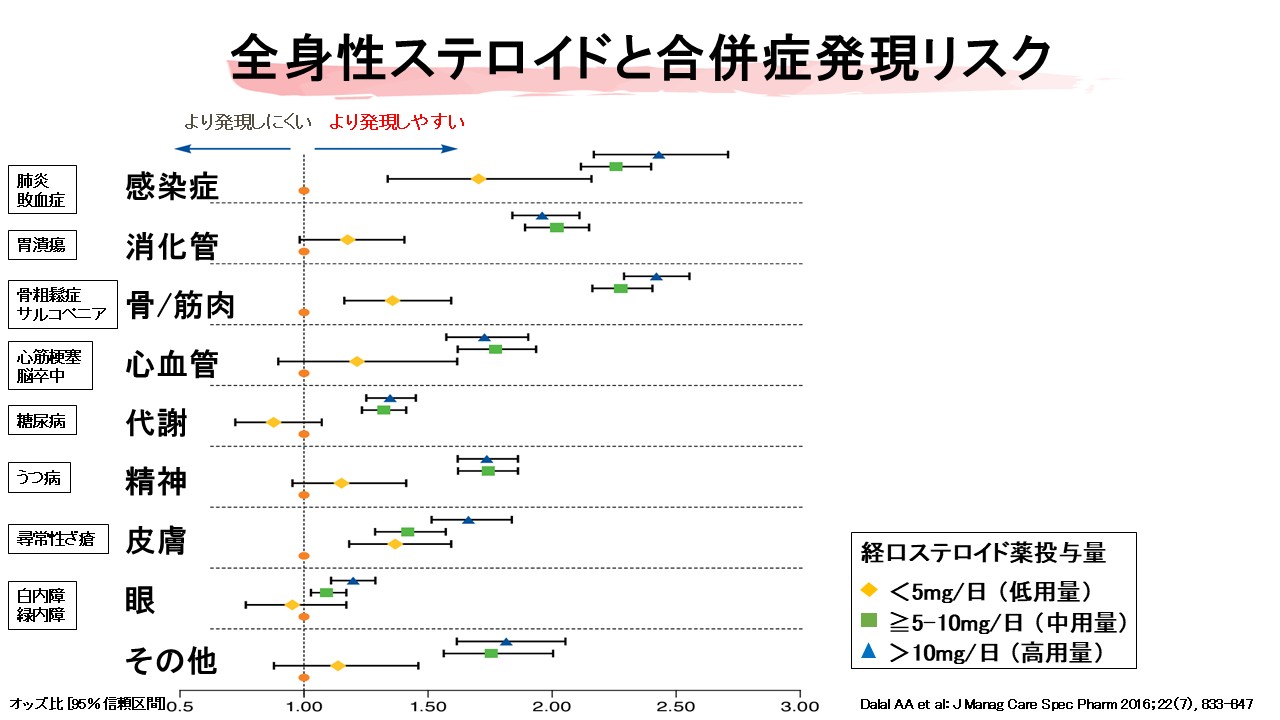
OCS累積量問題
近年、重症喘息診療で特に重視されているのがOCS累積投与量の概念である。従来は「短期のburstなら安全」と考えられがちであったが、複数の報告により、累積1000mg程度を超えるあたりから有害事象リスクが無視できなくなることが示されている【5】。プレドニゾロン換算で考えると、たとえば1回20〜30mg/日を5〜7日間投与するburstを年に2〜3回繰り返すだけでも、比較的短期間でこの域に到達し得る。つまり、患者が「たまに飲むだけ」と認識していても、医療者の視点ではすでに累積投与量がかなり進んでいることがある。ここに重症喘息診療の盲点がある。外来では、その時々の処方だけでなく、過去1年、2年単位でどれだけOCSを使ってきたかを見える化しなければならない。OCS累積量を患者と共有することは、「今月はこの薬で落ち着いた」という短期評価から、「この先の副作用リスクを減らす」という長期目標へ視点を移すうえで非常に有効である。そのため、近年の重症喘息治療では、単に症状やACT改善を目指すだけでなく、OCS sparing、すなわち全身ステロイド曝露そのものを減らすことが主要な治療目標として位置づけられている。生物学的製剤の意義も、単に増悪を減らすことだけでなく、OCS累積量を減らし長期有害事象を避ける点にある。
重症喘息の免疫学的病態
重症喘息の理解には、その免疫学的背景を把握することが重要である。近年、喘息の多くはType2炎症を基盤としていることが明らかとなった【6】。Type2炎症では、気道上皮がウイルス感染、アレルゲン、たばこ煙、PM2.5、黄砂などの刺激を受けることで、TSLP、IL-33、IL-25といったアラーミンを放出する。これらは自然免疫系のILC2、さらに獲得免疫系のTh2細胞を活性化し、IL-4、IL-5、IL-13などのサイトカイン産生を促進する。IL-4はIgE産生に関与し、IL-5は好酸球の分化・生存・活性化を支え、IL-13は粘液分泌や気道過敏性亢進に関与する。こうした炎症カスケードが継続することで、好酸球性炎症、気道浮腫、粘液過剰分泌、気道平滑筋収縮、さらには気道リモデリングが進行する。結果として、患者は症状を繰り返し、増悪しやすくなり、標準吸入治療のみでは抑えきれない病態に陥る。一方で、喘息はすべてがType2炎症で説明できるわけではない。好中球優位、肥満関連、喫煙関連など、Type2 lowの要素が前景に出る患者も存在する。このような多様性が、重症喘息を一つの疾患として画一的に扱えない理由であり、フェノタイプ評価の重要性につながる。
重症喘息フェノタイプ分類
重症喘息は一様な疾患ではなく、複数のフェノタイプが存在する。日常診療では、少なくとも以下のような視点で整理すると理解しやすい。
1)好酸球性喘息
血中好酸球数高値、FeNO高値、増悪反復を特徴とし、Type2炎症が前景にある。IL-5経路やIL-4/13経路が病態に深く関与する症例が多く、生物学的製剤の反応性が期待しやすい。
2)アレルギー性喘息
IgE高値、通年性アレルゲン感作、若年発症などを特徴とする。オマリズマブの適応検討に直結しやすいが、好酸球性炎症を同時に伴う症例も少なくなく、単一軸で判断できないことも多い。
3)Type2 high / ECRS合併喘息
FeNO高値、好酸球増多、鼻茸、嗅覚障害、副鼻腔病変などを伴う症例では、上気道・下気道をまたぐType2炎症が想定される。デュピルマブが有力候補となることが多い。
4)Type2 low / 好中球性喘息
好酸球やFeNOが高くなく、感染、喫煙、肥満、気流制限固定化などが背景にあることが多い。既存のType2標的治療が必ずしも当てはまりにくく、テゼペルマブのような上流分子標的が選択肢となる場合がある。
5)肥満関連喘息
肥満、睡眠障害、逆流、身体活動低下、心理社会的要因が絡み合い、症状が強くても炎症バイオマーカーが必ずしも高くないことがある。純粋な炎症制御だけではなく、併存症介入が重要となる。実際の患者はこれらのフェノタイプのいずれか一つにきれいに収まるわけではなく、好酸球性でありながらアレルギー性を併せ持ち、さらにECRSを合併するなど、重なり合いが多い。したがって、フェノタイプ分類はラベル貼りのためではなく、生物学的製剤選択や説明の方向性を整理するための臨床的道具として用いるべきである。
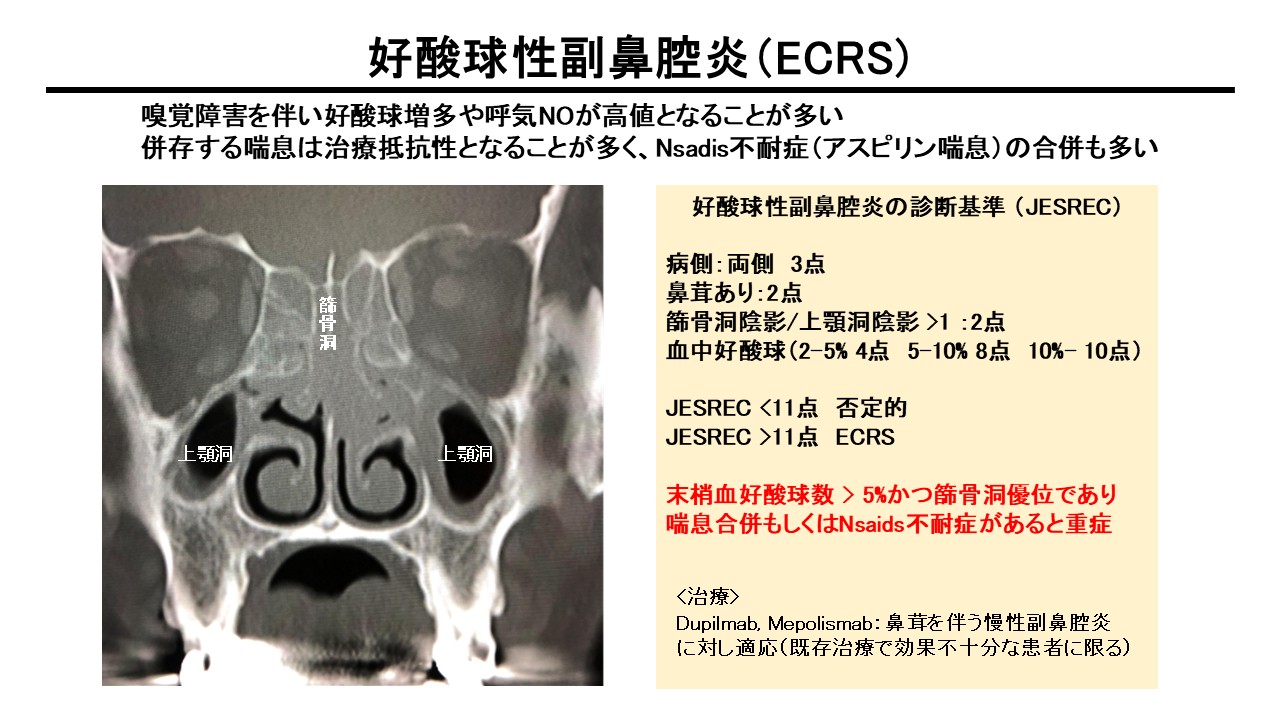
好酸球性副鼻腔炎(ECRS)と重症喘息
重症喘息診療では、下気道だけでなく上気道病変を評価する視点が極めて重要である。なかでも好酸球性副鼻腔炎(Eosinophilic Chronic Rhinosinusitis: ECRS)は、重症喘息と強く関連する重要な併存症である。ECRSは好酸球優位の慢性副鼻腔炎であり、鼻茸形成、嗅覚障害、篩骨洞優位病変、血中好酸球増多などを特徴とする。日本ではJESREC studyにより診断基準・分類が整備されている【13】。JESRECスコアは、両側病変、鼻茸、篩骨洞優位陰影、血中好酸球割合などから構成され、一定点数以上でECRSの可能性が高いと判断される。さらに、末梢血好酸球増加や喘息合併、NSAIDs不耐症などを伴う場合には重症度も高くなりやすい。ECRS合併喘息では、FeNO高値、好酸球増多、鼻閉、後鼻漏、嗅覚障害などが臨床ヒントとなる。このような患者では、上気道・下気道を通じてType2炎症が強く持続している可能性が高い。したがって、治療方針を考える際には「喘息の薬を選ぶ」だけでなく、「副鼻腔炎も含めて全身のType2炎症をどう抑えるか」という視点が必要になる。デュピルマブやメポリズマブは鼻茸を伴う慢性副鼻腔炎にも適応を有しており、喘息と副鼻腔炎の双方を改善しうる点で重要な選択肢である【14】。重症喘息患者で鼻症状があるにもかかわらず上気道評価が十分でないケースは少なくない。耳鼻科との連携により副鼻腔CTや鼻内所見を確認することは、生物学的製剤選択における大きな助けとなる。実臨床では、ECRSの存在がデュピルマブを選ぶ有力な根拠となることが多い。
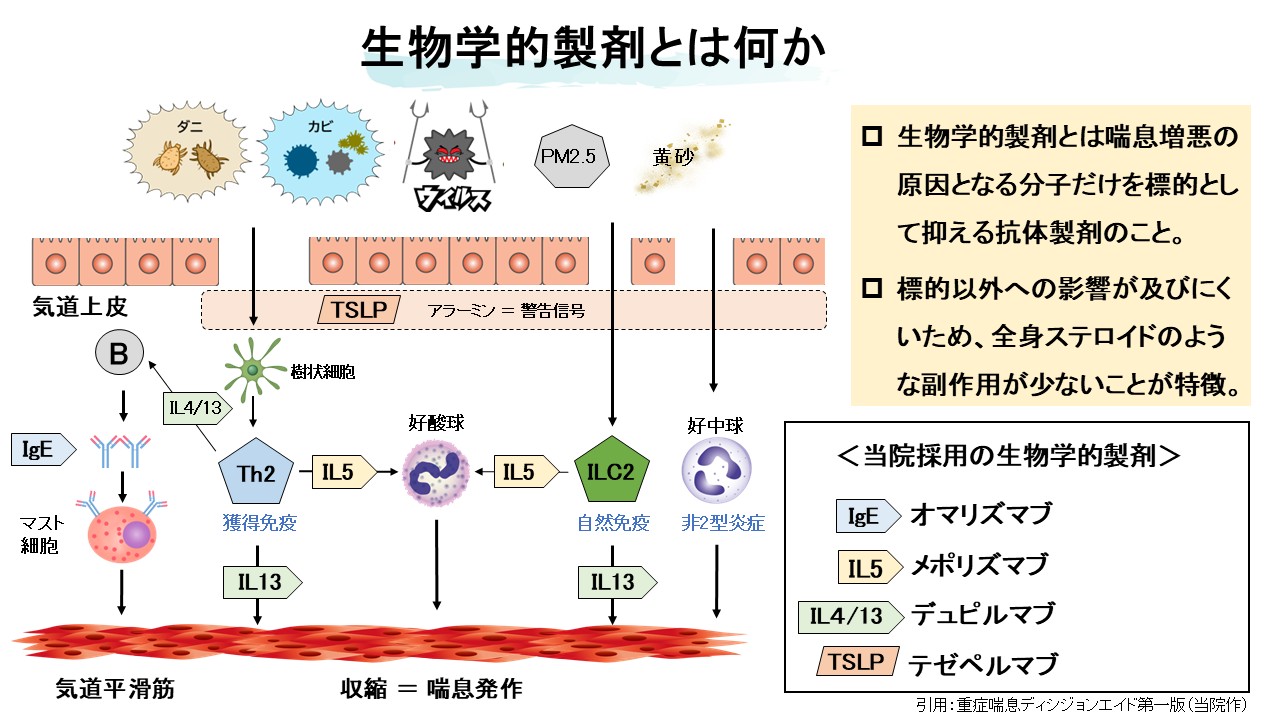
生物学的製剤とは何か
生物学的製剤とは、喘息増悪や炎症に関与する特定の分子を標的として抑制する抗体製剤である。標的分子以外への影響が比較的少ないため、全身ステロイドのように広範な副作用を来しにくいことが特徴である。現在、重症喘息に対して臨床的に重要な標的は、IgE、IL-5、IL-4/13、TSLPである。オマリズマブはIgEを標的とし、アレルギー性喘息に用いられる。メポリズマブはIL-5経路を抑制し、好酸球性炎症を減弱させる。デュピルマブはIL-4/13シグナルを阻害し、FeNO高値やECRS合併例でも有効性が期待される。テゼペルマブは上流のアラーミンであるTSLPを標的とし、好酸球数に依存しない比較的幅広い効果が期待される。これらの薬剤は共通して、増悪抑制、症状改善、QOL改善、OCS使用量減少を目標とするが、どの患者にどの薬剤が最も適しているかは一律ではない。そのため、炎症バイオマーカー、併存症、投与方法、通院間隔、患者の希望、費用負担などを総合的に評価する必要がある。
生物学的製剤の臨床試験エビデンス
重症喘息に対する生物学的製剤の有効性は、複数の大規模臨床試験により示されている。メポリズマブのDREAM試験では、重症好酸球性喘息において年間増悪率が有意に減少した【7】。IL-5を標的とする治療が、好酸球優位の増悪反復例に強い意義を持つことを示した代表的研究である。デュピルマブのQUEST試験では、増悪率低下に加えて肺機能改善も示され、FeNO高値や好酸球高値の症例において特に有効性が期待されることが示唆された【8】。また、上気道疾患を伴う患者では臨床的な満足度が高いこともしばしば経験される。テゼペルマブのNAVIGATOR試験では、好酸球数にかかわらず増悪率を有意に低下させたことが注目された【9】。これは、Type2 high症例のみならず、従来のバイオマーカーで捉えにくい症例にも一定の効果が期待できる可能性を示している。こうした試験成績は、生物学的製剤が単なる“新しい高価な薬”ではなく、重症喘息治療戦略を根本から変え得る治療であることを裏づけている。
バイオ製剤選択アルゴリズム
実臨床で薬剤選択を考える際には、単一の指標だけで決めるのではなく、いくつかの情報を組み合わせる必要がある。以下はあくまで臨床的な整理の一例である。
IgE高値・通年性アレルゲン感作が前景にある場合
アレルギー性喘息の要素が強く、適応条件を満たす場合はオマリズマブが候補となる。
血中好酸球高値・増悪反復が目立つ場合
好酸球性喘息としてIL-5阻害薬が有力候補となる。増悪抑制やOCS sparingを重視する場面で適している。
FeNO高値、ECRS合併、鼻茸、上気道症状が目立つ場合
IL-4/13経路が関与している可能性が高く、デュピルマブが有力候補となる。
非Type2要素がある、あるいはバイオマーカーが典型的でない場合
テゼペルマブが選択肢となる。好酸球高値が乏しい症例、複数フェノタイプが混在する症例でも検討しやすい。しかし、実際には「IgEも高い」「好酸球も高い」「FeNOも高い」「ECRSもある」といった症例が少なくない。その場合は、どの病態を最も強く是正したいか、患者が最も困っている症状は何か、自己注射や通院が可能か、費用負担はどうかといった現実的要素も含めて判断することになる。したがって、“アルゴリズム”は機械的に薬を決めるためではなく、説明と整理のために使うのが実践的である。
重症喘息患者の意思決定支援とKOFU study
日本における重症喘息患者の生物学的製剤導入プロセスを考えるうえで参考になる研究がKOFU studyである【12】。この調査では、生物学的製剤施行中患者と、推奨されたが未施行の患者を比較し、患者背景、重症度認識、重視する項目、受容プロセスなどが検討された。興味深いのは、医師が認識している重症度と患者自身の認識に乖離がみられた点である。とくに未施行群では、自身が重症喘息であるという認識が十分でない患者が多かった。また、生物学的製剤未施行群では費用負担を強く重視する割合が高く、一方で施行群では長期的効果や日常生活改善を重視する傾向がみられた。さらに、患者が生物学的製剤を受け入れるまでには複数回の説明が必要なことが多く、「もっと早く知りたかった」「もっと早く始めたかった」と感じている患者が少なくないことも示された。これは、医師が一度提案して断られた時点で終わりにするのではなく、タイミングを見ながら繰り返し情報提供を行うことの重要性を示している。KOFU studyから実臨床に引き寄せて考えると、患者に伝えるべきことは少なくとも以下の4つに整理できる。すなわち、①患者自身が現在重症喘息であること、②生物学的製剤の効果、③OCSの長期リスク、④医療費制度を含む費用の見通し、である。これらを一度に詰め込むのではなく、患者が理解できる順序で段階的に伝えることが求められる。

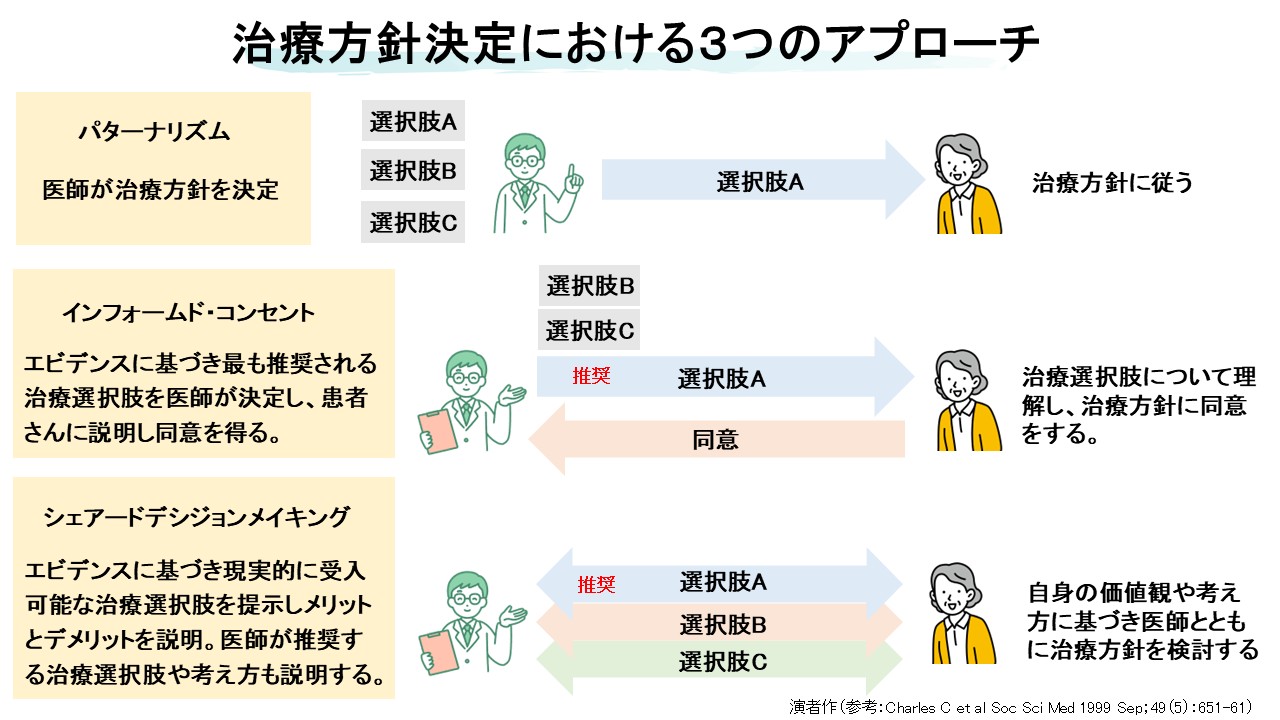
Shared Decision Making(SDM)とは何か
生物学的製剤導入の場面では、Shared Decision Making(SDM)が極めて重要となる。SDMとは、医師が一方的に治療方針を決めるパターナリズムでもなく、単に情報を提供して同意を得るインフォームド・コンセントでもない。医療者と患者がともに情報を共有し、患者の価値観や希望を踏まえながら、治療方針を共同で決定していくプロセスである【10】。Charlesらは、SDMの構成要素として、少なくとも医療者と患者の双方が意思決定に関与すること、情報が共有されること、希望の治療について合意形成を図ること、最終的な実施方針に合意することを挙げている【10】。重症喘息治療のように、複数の現実的選択肢があり、しかもそれぞれにメリット・デメリット・費用・価値観の違いが伴う場面では、まさにSDMが適したモデルである。SDMは患者満足度、治療アドヒアランス、意思決定後悔の低減に寄与することが報告されている【11】。また、ヘルスリテラシーが十分でない患者であっても、平易な言葉と構造化された説明を用いることで、意思決定参加や自己効力感を高められる可能性がある。つまり、SDMは“理解できる患者にだけ行う高度な会話”ではなく、むしろ理解支援が必要な患者ほど恩恵を受けるアプローチである。
Three-talk modelを用いた実践
SDMの実践モデルとして有用なのがElwynらのThree-talk modelである【11】。これは、Team talk、Option talk、Decision talkの3段階で構成される。
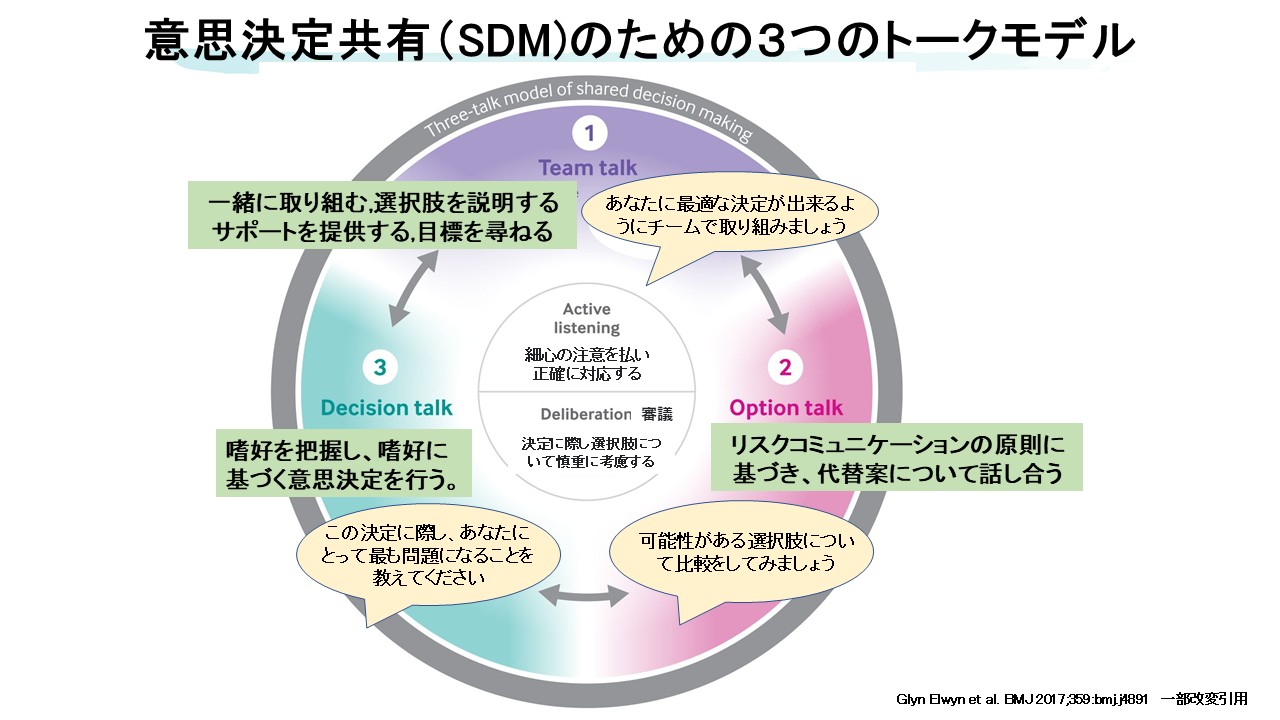
Team talk
まず、患者に「治療の選択肢があること」「一緒に考えていくこと」を伝える段階である。重症喘息では、「このまま今の治療を続ける」「OCSでその都度しのぐ」「生物学的製剤を導入する」といった現実的選択肢があり得ることを共有し、意思決定を患者に丸投げするのではなく、チームとして支える姿勢を示すことが大切である。
Option talk
次に、各選択肢のメリット・デメリットを比較しながら説明する。たとえば、生物学的製剤は増悪抑制やOCS減量が期待できる一方、通院・自己注射・費用が課題となる。OCS継続は一時的には楽になるが、長期的には副作用リスクが蓄積する。この段階では、数字や図を使って視覚化することが有効である。
Decision talk
最後に、患者の価値観を引き出して統合する。「今の話を聞いて、先生は何が一番気になりますか」「治療を選ぶうえで、何が一番大事ですか」といった問いを通じて、患者の優先順位を明らかにする。そのうえで、患者にとって納得できる選択肢を一緒に決めていく。ここで重要なのは、結論を急ぎすぎないことである。重症喘息患者が一度でバイオ導入を受け入れるとは限らず、再検討可能な余地を残すことも重要である。
多職種介入の重要性
生物学的製剤導入の意思決定支援は、必ずしも医師一人で完結させる必要はない。むしろ、看護師、医療事務、薬剤師、医療ソーシャルワーカーなど多職種が関与することで、患者理解や受容を支えやすくなる。KOFU studyでも、多職種介入が生物学的製剤導入プロセスに好影響を与える可能性が示唆されている【12】。実際、医師は病態説明や薬剤選択の判断に強みを持つ一方で、看護師は自己注射指導や不安への傾聴、事務スタッフは高額療養費制度や限度額認定証の案内など、異なる役割を担うことができる。患者にとっては、一度の診察だけで複雑な情報をすべて理解することは難しく、複数職種から同じ方向性でサポートを受けることで、理解が深まりやすい。

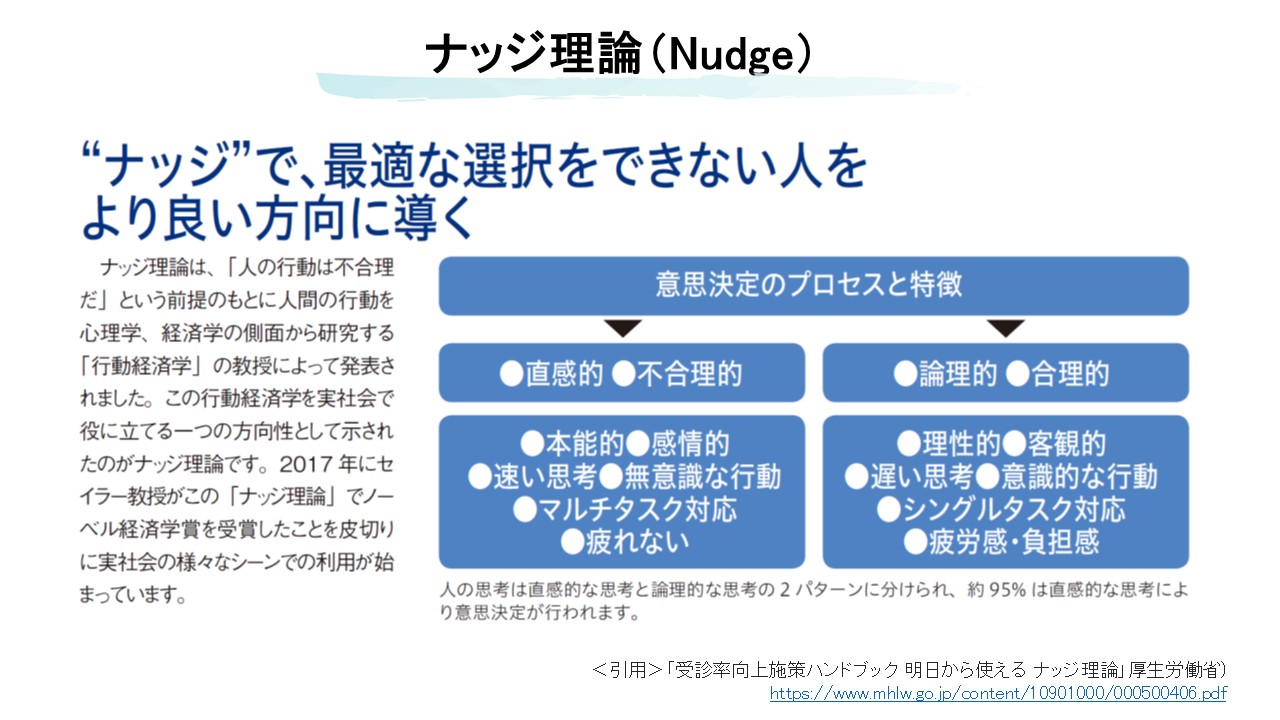
行動経済学と患者の意思決定バイアス
重症喘息患者の意思決定を難しくする要因として、行動経済学的バイアスがある。患者は必ずしも合理的に判断するわけではなく、感情や経験に大きく左右される。これは異常なことではなく、人間として自然な反応である。むしろ、こうしたバイアスを理解したうえで支援することが重要である。
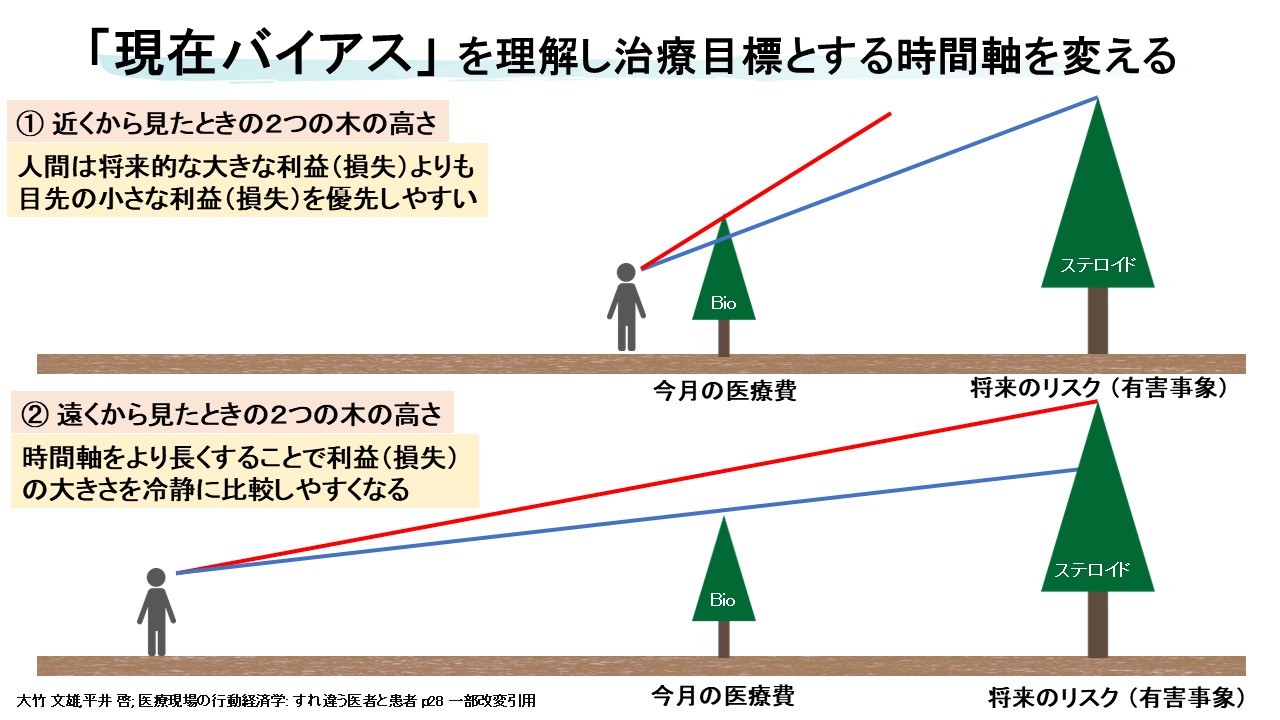
現在バイアス
現在バイアスとは、将来の大きな利益や損失よりも、目先の小さな利益や損失を優先しやすい傾向である。重症喘息では、「将来のOCS副作用」よりも「今月の医療費負担」が強く意識されやすい。生物学的製剤導入では、長期的な利益を理解してもらうために、時間軸を広げた説明が必要である。
現状維持バイアス
現状維持バイアスとは、新しい選択肢に伴う不確実性を避け、現状のままでいたいと感じる傾向である。「今までOCSでやってきた」「注射は大変そう」「副作用が心配」といった反応は典型的である。この場合、現状維持にもリスクがあること、すなわち“今のままでいることが安全とは限らない”ことを客観的データで示すことが重要になる。こうしたバイアスに対しては、メリット・デメリットを見える化し、段階的に提案し、結論を急がない姿勢が有効である。たとえば、SITT導入時に将来の選択肢としてバイオの存在を軽く触れておき、OCS1回目で予告し、2回目で本格提案するといった流れは、患者の心理的抵抗を和らげるのに有用である。

医療費説明の重要性
生物学的製剤導入の最大の障壁の一つは医療費である。したがって、費用説明は“補足事項”ではなく、意思決定支援そのものである。重症喘息患者に説明すべき主な制度として、高額療養費制度、限度額認定証、付加給付制度、医療費控除がある。

高額療養費制度
高額療養費制度は、1か月あたりの自己負担額に上限を設ける制度であり、所得区分によって上限額が異なる。多数回該当では4回目以降にさらに自己負担が軽減される場合がある。患者説明では、薬価そのものではなく、「実際に支払う上限額はいくらか」を具体的に示すことが重要である。
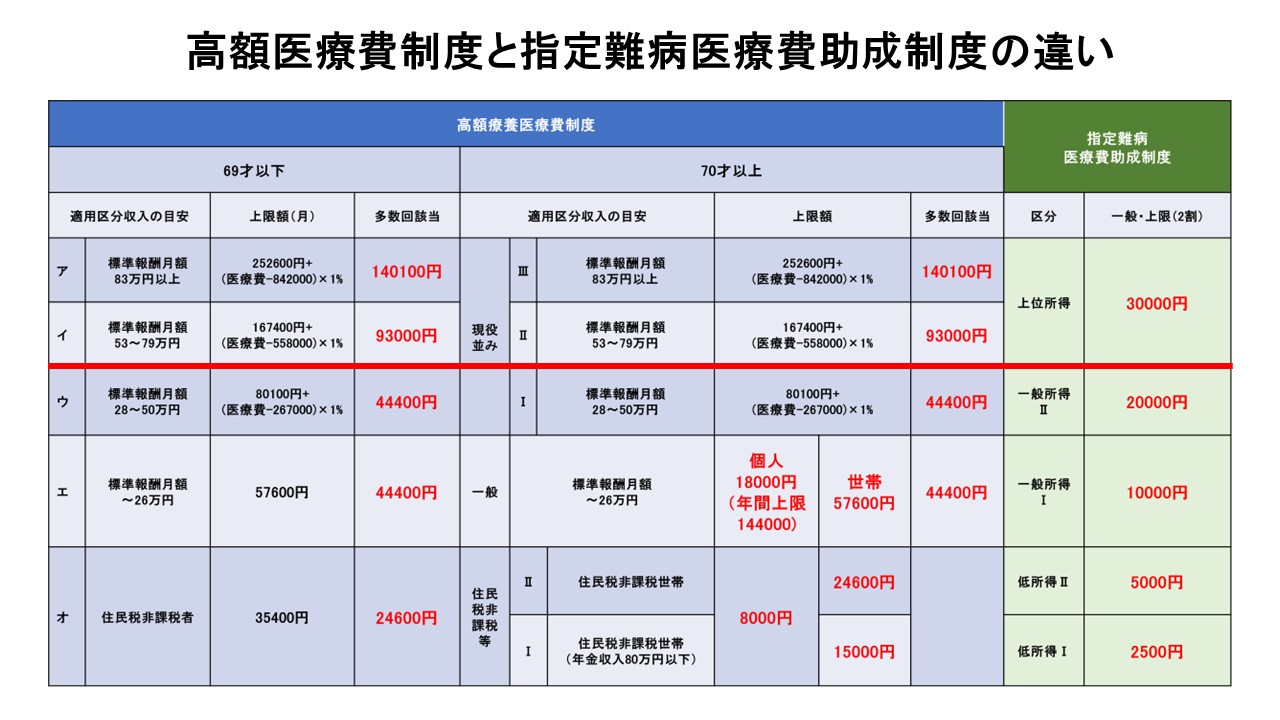
限度額認定証
限度額認定証を利用することで、窓口での支払いを自己負担上限額までに抑えることができる。現在はマイナ保険証の活用により、事前手続き不要となるケースも多いが、患者がその仕組みを理解していないことも多いため、医療機関側から積極的に案内する必要がある。
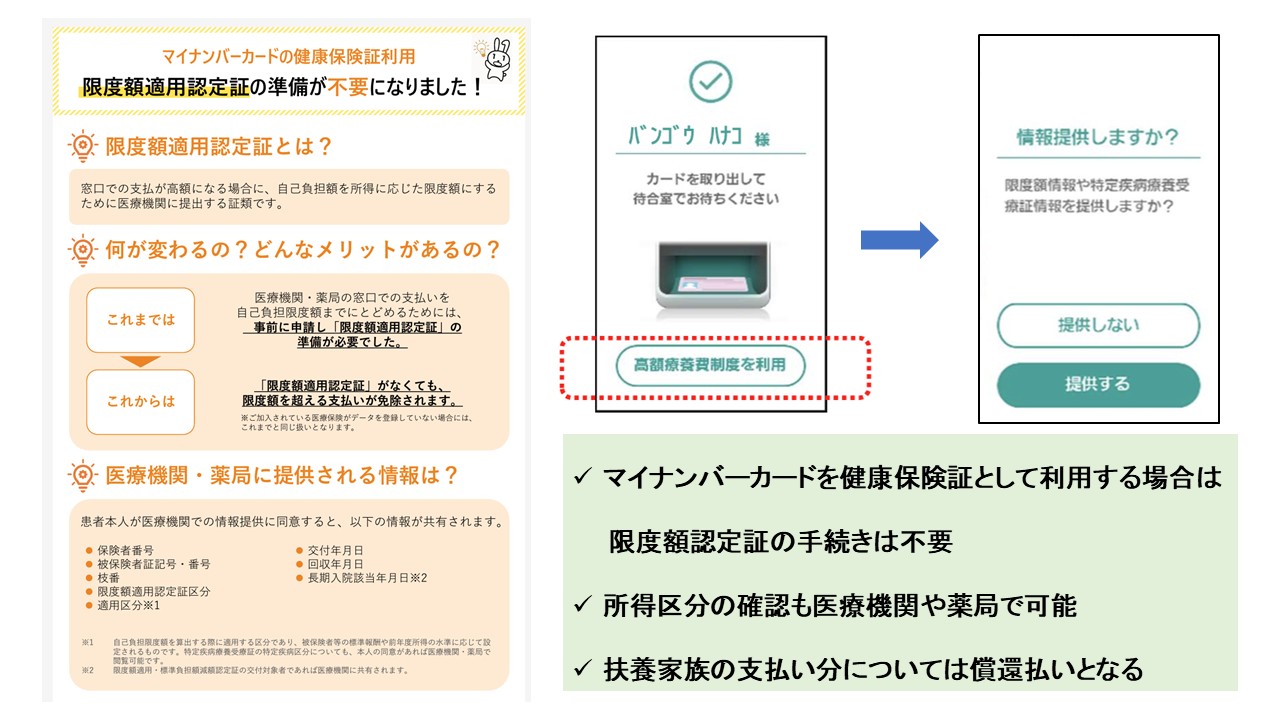
付加給付制度
大手企業の健康保険組合などでは、法定給付に加えて独自の付加給付制度があり、実質自己負担がさらに低く抑えられる場合がある。一方で、協会けんぽや国保では付加給付がないことも多い。したがって、保険種別を確認するだけでも医療費見通しは大きく変わる。

医療費控除
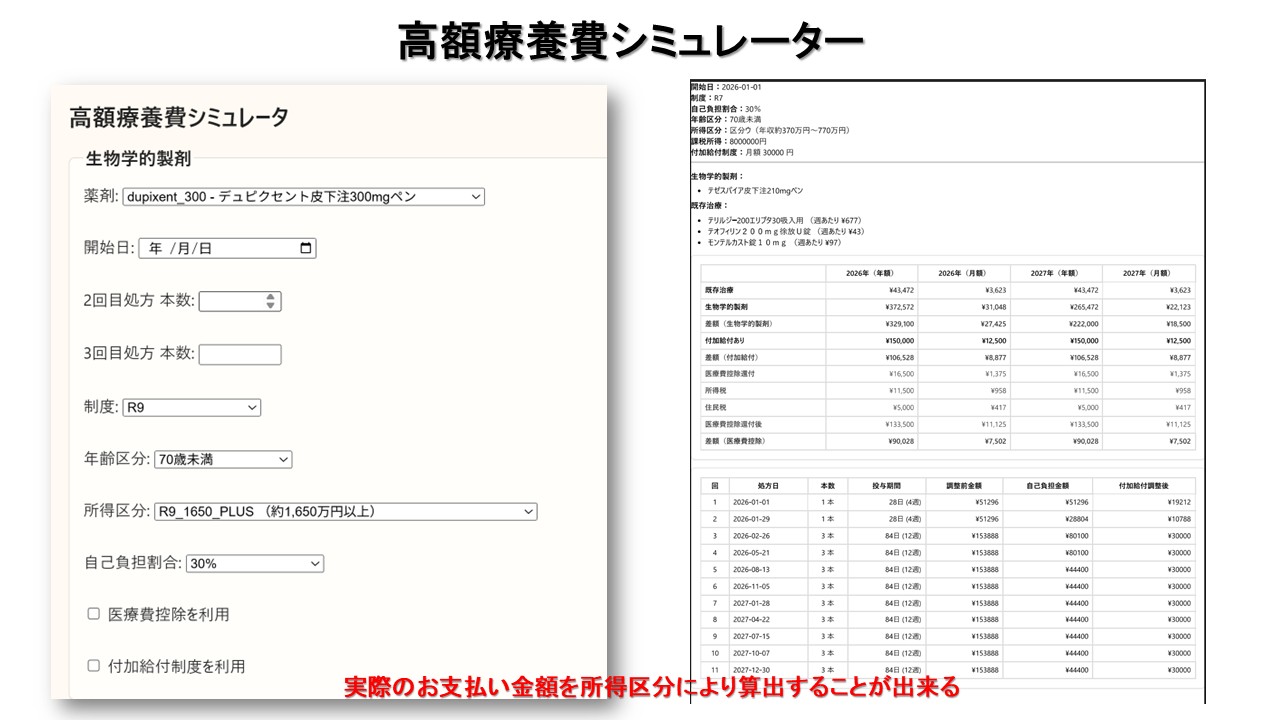
年間医療費が一定額を超える場合には、確定申告による医療費控除で還付を受けられる。とくに高額なバイオ治療では、年間支出ベースで考えると実質負担がさらに軽減される可能性がある。患者には月額だけでなく年額ベースで説明することが有用である。費用説明では、単に制度名を並べるだけでは不十分である。患者にとって重要なのは「自分はいくら払うのか」「何をすればその金額になるのか」「いつから減額されるのか」である。そのため、シミュレーターや表を用いて具体的に示すことが強力な支援となる。
症例提示
ここで、生物学的製剤導入を考えた典型的な症例を提示する。28歳女性。既往にうつ病がある。他院で喘息治療を受けていたが改善不十分で当院受診となった。初診時には喘鳴、呼吸苦を認め、高用量ICS/LABA/LAMAへの変更、LTRA追加、OCS burstを行った。検査では白血球9400、好酸球7.1%(667/μL)、総IgE 1500、ダニほか多数アレルゲン陽性、FeNO 83 ppbであった。治療経過として、Visit2では症状改善しFeNOは16 ppbまで低下したが、Visit3で再度増悪し、SRT追加と2回目のOCS burstを要した。この時点で所得区分の確認を行った。Visit4では所得区分エで付加給付制度なしと判明。Visit5でさらにOCS burstを要し、生物学的製剤導入のインフォームドコンセントを行った。この症例では、SITT、LTRA、必要時OCSにもかかわらず年2回以上のOCS投与が必要であり、重症喘息と判断できる。好酸球増多、FeNO高値、通年性アレルゲン陽性からType2炎症が示唆される。一方、治療後FeNOは低下しており、ECRS評価のための副鼻腔CTはこの時点で未施行であった。薬剤選択としては複数のバイオが候補になりうるが、病態、投与利便性、費用面などを総合し、最終的な選択を患者と共有しながら決定していくことになる。この症例のポイントは、単にバイオ適応を判断することではなく、OCS反復の時点で早めに費用確認を行い、患者の準備を整えている点である。重症喘息患者の意思決定支援は、適応が固まってから始まるのではなく、実はその前から始まっている。
重症喘息患者の実臨床導入フロー
重症喘息診療では、患者が初診時から直ちに生物学的製剤適応となることはむしろ少なく、通常は既存治療の最適化を段階的に行いながら導入を検討する。実臨床では、以下のような流れで考えると整理しやすい。
Step 1 吸入治療の最適化
まずは高用量ICS/LABAを基本に、吸入手技、アドヒアランス、吸入デバイスの適合性を確認する。症状不良を「薬が効かない」と決めつける前に、そもそも適切に吸えているか、継続できているかを見直す必要がある。
Step 2 SITT導入・既存治療の最大化
LAMA追加や単一吸入器三剤配合(SITT)を導入し、必要に応じてLTRAなども追加する。この段階で多くの患者はコントロール可能となるため、重症喘息診断には“最大限の既存治療”が実施されていることが前提となる。
Step 3 増悪の評価
それでもなお、OCS投与を年2回以上要する、入院・救急受診を繰り返す、普段の症状コントロールが悪い、といった場合には重症喘息を疑う。特にOCS年2回以上という基準は、患者自身にも説明しやすく、実臨床上の転換点になりやすい。
Step 4 フェノタイプ評価
血中好酸球数、FeNO、総IgE、アレルゲン感作、ECRSの有無、肥満、喫煙、睡眠障害、逆流などを評価する。ここで重要なのは、数値だけでなく、患者がどの病態に最も苦しんでいるかを把握することである。
Step 5 費用説明とSDM
適応が見えてきた段階で、高額療養費制度や付加給付制度を含む費用説明を行い、生物学的製剤導入の現実性を患者と共有する。この時点で初めて患者が前向きになることもあれば、逆に費用が壁となって慎重になることもある。いずれにしても、ここでSDMが重要となる。
Step 6 生物学的製剤導入
フェノタイプ、併存症、投与方法、通院頻度、自己注射可否、患者の価値観を踏まえて薬剤を選択する。導入後は、増悪頻度、ACT、肺機能、FeNO、OCS使用量などを用いて3〜6か月で治療効果を評価し、継続・変更を検討する。
このフローの本質は、バイオを“最後の切り札”として漫然と先送りするのではなく、OCS反復の時点で早めに選択肢として提示し、患者が理解・熟考する時間を確保することにある。
Take Home Message
重症喘息診療において、医療者の役割は患者に生物学的製剤を説得することではない。患者が自分の病状を理解し、増悪やOCSのリスクを認識し、費用も含めた現実的な条件を踏まえたうえで、自分にとって納得できる治療を選べるよう支援することである。そのためには、重症喘息の病態理解、フェノタイプ評価、ECRSを含む併存症評価、OCS累積量の把握、生物学的製剤のエビデンス理解、医療費制度の具体的説明、そしてShared Decision Makingの実践が必要となる。これらを統合して初めて、重症喘息患者に対する真の意思決定支援が実現する。重症喘息患者さんのために医療従事者に求められているのは、「患者さんに生物学的製剤治療を説得すること」ではない。「患者さん自身が生物学的製剤治療を行うかどうかを決めるために、必要な情報を提供し、意思決定できるように支援すること」である。この視点こそが、これからの重症喘息診療の中核になると考える。
引用文献
【1】Chung KF, Wenzel SE, Brozek JL, et al. International ERS/ATS guidelines on definition, evaluation and treatment of severe asthma. Eur Respir J. 2014;43:343-373.
【2】World Health Organization. Asthma. World Health Organization.
【3】Matsunaga K, Hirano T, Akamatsu K, et al. Progression of fixed airflow limitation in asthma: correlation with annual decline in FEV1. J Allergy Clin Immunol Pract. 2015;3:759-764.
【4】Dalal AA, Duh MS, Gozalo L, et al. Dose-response relationship between long-term systemic corticosteroid use and related complications in patients with severe asthma. J Manag Care Spec Pharm. 2016;22:833-847.
【5】Price DB, Trudo F, Voorham J, et al. Adverse outcomes from initiation of systemic corticosteroids for asthma: long-term observational study. J Asthma Allergy. 2018;11:193-204.
【6】Lambrecht BN, Hammad H, Fahy JV. The cytokines of asthma. Nat Immunol. 2019;20:12-24.
【7】Pavord ID, Korn S, Howarth P, et al. Mepolizumab for severe eosinophilic asthma (DREAM): a multicentre, double-blind, placebo-controlled trial. Lancet. 2012;380:651-659.
【8】Castro M, Corren J, Pavord ID, et al. Dupilumab efficacy and safety in moderate-to-severe uncontrolled asthma. N Engl J Med. 2018;378:2486-2496.
【9】Menzies-Gow A, Corren J, Bourdin A, et al. Tezepelumab in adults and adolescents with severe, uncontrolled asthma. N Engl J Med. 2021;384:1800-1809.
【10】Charles C, Gafni A, Whelan T. Decision-making in the physician-patient encounter: revisiting the shared treatment decision-making model. Soc Sci Med. 1999;49:651-661.
【11】Elwyn G, Durand MA, Song J, et al. A three-talk model for shared decision making: multistage consultation process. BMJ. 2017;359:j4891.
【12】Tamada T, et al. 重症喘息患者における治療および喘息症状についてのインターネット調査(KOFU study). Ther Res. 2021;42:853-860.
【13】Tokunaga T, Sakashita M, Haruna T, et al. Novel scoring system and algorithm for classifying chronic rhinosinusitis: the JESREC Study. Allergy. 2015;70:995-1003.
【14】Bachert C, Han JK, Desrosiers M, et al. Efficacy and safety of dupilumab in chronic rhinosinusitis with nasal polyps. N Engl J Med. 2019;381:55-65.
参考記事
・重症喘息の治療
・重症喘息に関する講演会に参加
・重症喘息患者さんの意思決定支援を考える講演会
・ゾレア(オマリズマブ)【喘息治療薬】
・テゼスパイア(テゼペルマブ)【喘息治療薬】
・ヌーカラ(メポリズマブ)【喘息治療薬】
・デュピクセント(デュピルマブ)【喘息治療薬】
・高額療養費制度とは?わかりやすくイラスト解説|高額治療でも安心な理由

葛西よこやま内科・
呼吸器内科クリニック
院長 横山 裕
医院紹介

| 住所 | 〒134-0084東京都江戸川区東葛西5丁目1-2 第二吉田ビル3階 |
|---|---|
| 東京メトロ東西線 浦安、西葛西より2分、南行徳より4分、行徳より6分、妙典より8分 |
|
| TEL | 03-3877-1159 |
3階(院長)
| 診療時間 | 月 | 火 | 水 | 木 | 金 | 土 | 日 |
|---|---|---|---|---|---|---|---|
| 08:30~12:30 | ● | ● | ● | - | ● | ▲ | - |
| 13:30~18:00 | ● | ● | ● | - | ● | - | - |
休診日:木・土(午後)・日・祝日
▲… 8:30〜14:00
※午前の受付は12:00までとなります。
4階(女性医師)
| 診療時間 | 月 | 火 | 水 | 木 | 金 | 土 | 日 |
|---|---|---|---|---|---|---|---|
| 08:30~12:30 | ● | ● | ● | - | ● | ▲ | - |
| 13:30~16:30 | ● | ● | ● | - | ● | - | - |
休診日:木・土(午後)・日・祝日
▲… 8:30〜13:00
※午前の受付は12:00までとなります。





